Medicina Basada en la Evidencia, Información y Resultados del Proceso
¿Cómo se aprecia críticamente la Información y cómo se aplican los resultados del Proceso?
Culminado el paso precedente, Usted va a tener en su poder uno o varios resúmenes o abstracts. La actividad a seguir consiste en realizar una primera preselección, tratando de elegir aquellos que, a la luz del resumen, se vean más compactos, con mayores fortalezas metodológicas (posiblemente por su diseño) y que sean fácilmente accesibles. Esto puede encontrar dos tipos de obstáculos: Hasta no hace mucho la mayoría de los resúmenes no eran estructurados, o sea que no se consignaban los métodos desarrollados y como veremos más adelante, es allí donde se puede determinar la validez de un trabajo científico34. El segundo obstáculo, de trascendencia grande en nuestras latitudes, es la dificultad para obtener el texto completo del artículo encontrado. La alternativa para esto último, en ocasiones onerosa y que desborda las capacidades y recursos de algunas búsquedas, es la solicitud por vía electrónica de tales artículos in extenso.
Una vez se tiene el o los artículos, procede a continuación la lectura crítica para determinar su calidad e impacto. A medida que las estrategias de investigación clínica han ido perfeccionándose y “purificándose”, han hecho lo propio las estrategias tanto para leer críticamente la literatura como para aplicar los resultados obtenidos. Varias agremiaciones norteamericanas y británicas, encabezadas por los promotores y practicantes de la MBE consolidados en el Grupo de Trabajo de Medicina Basada en la Evidencia, han ido emitiendo en forma periódica desde hace 20 años, una serie de publicaciones en revistas55-57, y en libros15,58, tendientes a guiar la lectura de la literatura.
Cada una de la Guías se plantean acordes con el tipo de diseño empleado en los diferentes trabajos y a las que se debe referir el lector en caso de que se desee profundizar más en ese aspecto. En el caso de las “Guías del Usuario de la Literatura Médica” de JAMA, por ejemplo, han aparecido desde su primera emisión en 199356, cerca de 20 escritos, que iniciaron con los estudios primarios, vale decir, de intervenciones59,60, pruebas diagnósticas61-62, riesgo63 y pronóstico64, y continuaron con estudios secundarios como overviews65, análisis de decisiones66-67, estudios económicos68-69, y Guías de Práctica Clínica70-71, entre otros.
En términos generales, la apreciación y aplicación de los artículos contempla tres aspectos: 1. Establecer si el artículo es válido, o sea si está libre de sesgos o con una “dosis” tolerable de ellos. 2. Determinar qué calidad, cantidad y trascendencia de resultados fueron encontrados. 3. Definir la aplicabilidad de esos resultados en nuestro ejercicio.
Si bien profundizar en los numerales 2 y 3, escapa de los objetivos específicos de este capítulo, es pertinente decir aquí que en cuanto a la calidad, cantidad y precisión de los resultados (numeral 2) debería darse relevancia a aquellos resultados Clínicamente significativos por encima, y si bien importantes, de lo estadísticamente significativos. De la misma manera, en referencia a la aplicabilidad de los resultados, no podría existir una regla de oro que estuviera en capacidad de indicarle a Usted cómo sería la mejor manera de utilizar la información obtenida en su escenario de trabajo, con sus pacientes y con sus limitaciones y posibilidades.
Refiriéndonos puntualmente al primer punto, la validez de un artículo depende fundamentalmente de los materiales y métodos empleados en su desarrollo y sobre todo del diseño utilizado. Cada tipo de diseño obedece a ciertas necesidades, intenta responder preguntas específicas, persigue objetivos diferentes, tiene aplicaciones particulares y muestra fortalezas y limitaciones. Por ello, no todos los diseños van a producir resultados o evidencia de igual valor72.
Recientemente se le ha otorgado una gran atención a los niveles de evidencia, en los cuales se basan las recomendaciones para la práctica clínica, derivados de los procesos de investigación y adquisición de conocimiento. Diseños de gran validez y fortaleza, proporcionarán evidencia igualmente válida, de fácil difusión y aceptación, y con la capacidad de modificar las prácticas clínicas73,74,75.
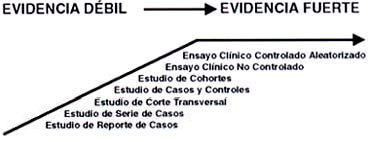
El orden de los diferentes diseños, en cuanto a la fortaleza de la evidencia que proporcionan, se muestra en la gráfica 7 72. En el nivel de mayor importancia dentro del proceso de captura de conocimientos científicos encontramos la observación controlada a través de un experimento76 , y su más acabada expresión es, en la actualidad, el Ensayo Clínico Controlado Aleatorizado Enmascarado (Randomized Clinical Trials o RCT del inglés). Este diseño, cuando quiera que es factible, sigue unos principios que buscan reducir la variación de factores extraños, diferentes a aquellos bajo estudio, reconoce y controla a priori las fuentes de error, controla los factores de confusión y está en capacidad de medir con relativa certidumbre el efecto del azar en los resultados obtenidos 72.
Gráfica No 7. Escalafón de los diversos tipos de investigación en cuanto a su fortaleza.
Con permiso de sus autores 72. Explicación en el texto.
Desde esta perspectiva, la evidencia así obtenida es considerada como seria, válida y de gran fortaleza y las recomendaciones de manejo derivadas de ella son de la mayor calidad. Sin embargo, algunas limitaciones éticas, económicas, técnicas, o de la naturaleza misma de la pregunta de investigación, imposibilitan la realización de un ensayo clínico en todos los casos, por lo que se debe recurrir a otras modalidades de diseño para contestar o generar ciertas preguntas (hipótesis) o encontrar la evidencia que apoye las decisiones a tomar. Es obvio que la incertidumbre en el momento de tomar decisiones es menor cuando en determinado tópico existe este tipo “excelso” de evidencia y no, por ejemplo, sólo Series de Casos. Desafortunadamente la vida real no es así, en la mayoría de las condiciones no se tiene tan sólida evidencia como se quisiera y entonces hay que recurrir a las limitadas pruebas existentes, pero colocándolas en su justo contexto que en definitiva es el papel preponderante de la MBE.
En este orden de ideas, MBE ha propuesto un sistema clasificatorio de la evidencia con base en su validez 73, 74, 75 y que, con algunas diferencias de literalidad empleados por los diferentes autores, sigue los lineamientos consignados en la tabla 1.
Tabla No. 1 Niveles de evidencia y grados de recomendación
Tabla No 1. Convenciones
| * Revisión Sistemática £ Guías de Práctica Clínica † Por homogeneidad de una revisión sistemática significa que ella está libre de variaciones preocupantes (heterogeneidad) en las direcciones y grados de los diferentes estudios individuales. No todas las revisiones sistemáticas con heterogeneidad estadísticamente significativa necesitan ser preocupantes, y no todas las heterogeneidades preocupantes necesitan ser estadísticamente significativas. Como se anotó arriba aquellas revisiones que muestran heterogeneidad preocupante deberían ser rotuladas con una “-” al final de su nivel designado. ‡ Ensayos Clínicos Controlados Aleatorizados @ Un apropiado espectro es una cohorte de pacientes0 en quienes normalmente podría ser realizada la prueba para la enfermedad en cuestión. Un inapropiado espectro compara pacientes ya conocidos de tener la enfermedad de interés con pacientes diagnosticados con otras enfermedades o condiciones. ¶ EsPoCon significa que en pruebas diagnósticas altamente Específicas un resultado Positivo Confirma la condición. y SeNeDes significa que en pruebas diagnósticas altamente Sensibles un resultado Negativo Descarta la condición |
¥ Se obtiene cuando todos los pacientes morían antes de que la intervención viniera a estar disponible, pero ahora alguno sobrevive con esta; o cuando algunos pacientes morían antes de que la intervención viniera a estar disponible pero ahora ninguno muere con ella. ** Pobre calidad en una cohorte significa que se falló claramente en definir los grupos de comparación y/o se falló en medir la exposición y el resultado en forma igual (preferiblemente enmascarado) y objetivo tanto en los expuestos como en los no expuestos y/o se falló en identificar o controlar adecuadamente por factores de confusión conocidos y/o se fallo en realizar un seguimiento suficientemente prolongado y completar el seguimiento de los pacientes. Pobre calidad en Casos y Controles significa que se falló claramente en definir los grupos de comparación y/o se falló en medir la exposición y el resultado en forma igual (preferiblemente enmascarado) y objetivo tanto en los casos como en los controles y/o se falló en identificar o controlar adecuadamente por factores de confusión conocidos. *** Pobre calidad en un estudio de cohorte pronóstica significa existe cuando hubo un muestreo sesgado a favor de los pacientes que ya tenían el resultado de interés, o la medición del resultado fue posible en menos del 80% de los pacientes estudiados, o los resultados fueron determinados de manera no enmascarada, de forma no objetiva, no hubo corrección por factores de confusión. |
La graduación aplicó inicialmente a las intervenciones pero pudo extenderse (con ciertas modificaciones) a los estudios observacionales analíticos y de pruebas diagnósticas. En este sentido, cada nivel de evidencia sustenta un grado correspondiente de recomendación en salud que, igualmente con pequeñas diferencias, sigue la esencia de lo expresado en la tabla 2.
Tabla No 2. Niveles de recomendación con base en la evidencia disponible.
Modificado y adaptado de CooK DL 73 , Sackett DL 74 y US Department of Health Services 75.
Recomendación Grado A: Existe evidencia satisfactoria que sustenta la recomendación para la condición /enfermedad / situación bajo consideración. En situaciones muy especiales ésta puede surtirse de evidencia de niveles 2 ó 3 cuando el evento es mortalidad, especialmente ante una enfermedad previamente fatal.
Recomendación Grado B: Existe evidencia razonable que sustenta la recomendación para la condición / enfermedad / situación bajo consideración.
Recomendación Grado C y D: Existe pobre o muy pobre evidencia (respectivamente) que sustenta la recomendación para la condición / enfermedad / situación bajo consideración.
Para determinar, después de haberse originado una pregunta y haber montado un proceso para responderla, se tendrá como resultado diversas combinaciones de la validez en su contexto de los trabajos existentes y de los resultados y aplicaciones de ellos. De esta manera podrán tenerse, entre otras, algunas de las siguientes respuestas: “….la evidencia encontrada tiene algunos problemas de validez que por lo tanto impiden ser confiados con la magnitud de los resultados obtenidos…”, “…serios errores metodológicos invalidan totalmente los resultados…”, “…hay fuerte evidencia, sólidamente construida, sin embargo los resultados no son clínicamente significativos….”, “…hay razonable evidencia al respecto, sin embargo las características de los pacientes en los diversos trabajos, difieren de los míos y por lo tanto no podría extrapolar los resultados a mi práctica…” o
“…..existe fuerte evidencia que apoya la administración eficaz y segura del medicamento a los pacientes que a diario veo en el hospital….”.
¿Cuáles podrían ser las conclusiones?
La MBE no es una nueva forma de Medicina. Es una herramienta eficiente de actualización y aprendizaje. No intenta desplazar el proceso tradicional de ejercicio clínico, sino fortalecerlo y robustecerlo con una imagen no sesgada de la evidencia existente.
La gran moraleja que se desprende de los resultados de la búsqueda y análisis de la evidencia existente y de la práctica profesional, es el de ser escépticos, críticos y con ánimo reflexivo sobre el proceso y las decisiones que se toman en el ejercicio clínico diario. El punto neurálgico es someter a evaluación toda la práctica que estamos ejerciendo, sea para refrendarla, reafirmarla o abandonarla.
Si se ha dado la lectura de las líneas anteriores de la manera como quisimos expresarlo, el lector podrá optar por una de tres opciones: Adoptarla, adaptarla o rechazarla. Para las dos primeras se deberá estar a la caza, de hoy en adelante, de momentos y espacios que le permitan adquirir las habilidades y lo capaciten en esta herramienta de aprendizaje, actualización y para el cuidado de los pacientes. Para la última medida se podrá optar libremente, ni más faltaba, pero habiendo tenido ya un conocimiento de causa para ello.
Como lo repetimos en los seminarios en que hemos participado hasta la fecha, pretendemos que, en aquellos interesados, éstas líneas se conviertan en la semilla para un dominio de la técnica. Estará en cada uno de los que emprendan esta tarea el de fertilizarla y nutrirla a fin de que germine, crezca y se desarrolle. En este sentido, se deberá realizar un inventario y evaluación personal de las dificultades y debilidades que se tengan en todas o en algunas de las cuatro partes del ciclo (construcción de preguntas – Búsqueda y Obtención de la literatura – Análisis Critico de ella – Aplicación de la Evidencia) para tratar de sobrellevarlas o adquirir las destrezas y habilidades necesarias para fortalecerlas.
La experiencia clínica fuertemente matizada por el juicio, la pericia, el ajuste a los deseos de los pacientes y la evidencia disponible obtenida a través de un proceso de actualización continuo, redundarán sin duda en el arte, disciplina o profesión78 de la medicina y por sobre todo en el bienestar de los pacientes a nuestro cuidado.
Bibliografía
- Grimshaw J, Eccles M, Russell I. Developing Clinically Valid Practice Guidelines. J Eval Clin Prac 1995; 1: 37 – 48
- Shin JH, Haynes RB, Jhonston ME. Effect of problem-based, self directed undergraduate education on life-long learning. Can Med Assoc J 1993; 148:969 – 76.
- Pardo R, Gamarra G. Fuentes, búsqueda, análisis de información y calidad de la evidencia: Breve introducción a la Medicina basada en la Evidencia. Rv Fac Med U Nal 1999;47(3):170-75.
- Morley CJ, Bangham AD, Miller N, Davis JA. Dry artificial lung surfactant and its effect on very premature babies. Lancet 1981; 1 (8211): 64 – 68.
- 5. Kellner JD, Ohlsson A, Gadomski AM, Wang EEL. Bronchodilatador therapy in Broncholitis (Cochrane Review). In: Cochrane Collaboration. Cochrane Database of Systematic Review, 4nd issue, 1998. BMJ Publishing Group, BMA House, Tavistock Square, London WC1H 9JR, UK.
- Lefering R, Neugebauer EA. Steroid controversy in sepsis and septic shock: a meta-analysis. Crit Care Med 1995;23(7): 1294 – 1303.
- Alderson P, Bunn F, Lefebvre C, Li Wan Po A, Li L, Roberts I, Schierhout G. Albumin administration in critically ill patients (Cochrane Review). In: Cochrane Collaboration. Cochrane Database of Systematic Review, 4nd issue, 1998. BMJ Publishing Group, BMA House, Tavistock Square, London WC1H 9JR, UK.
- Schierhout G, Roberts I, Alderson P. Colloids vs crystalloids in fluid resuscitation. (Cochrane Review). In: Cochrane Collaboration. Cochrane Database of Systematic Review, 4nd issue, 1998. BMJ Publishing Group, BMA House, Tavistock Square, London WC1H 9JR, UK.
- Weiss V, Needlman R. To teach is to learn twice. Resident teachers learn more. Arch Paediatr Adolesc Med 1998;152 (2): 190 -2.
- Sumer T, Taylor DK, McDonald M, Gillard M, Grasel K, Kaplan W, Kherellah N. The effect of anticipatory discharge orders on legth of hospital stay in staff pediatric patients. Am J Med Qual 1997;12(1): 48 – 50.
- Hickson GB, Altemeier WA, Perrin JM. Physician reimbursement by salary or fee-for-service: effect on physician practice behavior in a randomized prospective study. Pediatrics 1987;80(3): 344 –350.
- Solomon MJ, McLeod RS. Surgery and the randomised controlled trial: past, present and future. Med J Aust 1998; 169: 380 – 83.
- McClarey M. Implementing clinical effectiveness. Nursing Management 1998;5:16 – 19.
- Grahame-Smith D. Evidence base medicine: Socratic dissent. BMJ 1995; 310 : 1126 – 28.
- Sackett DL, Richardson WS, Rosenberg W, Haynes RB. Evidence Based-Medicine: How to Practice & Teach EBM. 1ª Edición. Londres UK. Churchill Livingstone. 1997: 1 – 36.
- Rosenberg W, Donald A. Evidence Based Medicine: an approach to clinical problem-solving. BMJ 1995; 310 : 1122 – 1126.
- Evidence Based Medicine Working Group. Evidence based-medicine: A new approach to teaching the practice of medicine. JAMA 1992; 268: 2420 – 25.
- Rodríguez A. Panorama de la informática y telemática médicas. Rev Fac Med U Nal 1997;45(4):187-88.
- Antman EM, Lau J, Kupelnick, Mosteller F, Chalmers TC. A Comparison of Results of Meta-analyses of Randomized Control Trials and Recommendations of Clinical Experts: treatment for Myocardial infarction. JAMA 1992; 268(2): 240- 48.
- Haynes RB. Where’s the meat in clinical journals?. ACP Journal Club 1993;119: A23-24.
- Davidoff F, Haynes RB, Sackett DL, Smith R. Evidence Based Medicine: A new journal to help doctors identify the information they need. BMJ 1995; 310:1085 – 6.
- Weed LL. New connections between medical Knowledge and patient care. BMJ 1997;315:231 – 235.
- Echeverry J. Medicina basada en la evidencia. Entre la tiranía y la actualización. XXXIV Congreso Nacional de Urología. Sociedad Colombiana de Urología. Ibagué, 1999.
- Hills G. The Knowledge disease. BMJ 1993;307:1578 – 1578.
- Covell DG, Uman GC, Manning PR. Information Needs in Office Practice: Are they Being Met?. Ann Intern Med 1985; 103: 596 – 99.
- Davis A, Thompson MA, Oxman AD. Changing Physician Performance: A systematic review of the effect of continuing medical education strategies. JAMA 1995; 274(9):700-5.
- Cantillon P, Jones R. Does continuing medical education in general practice make a difference? BMJ 1999; 318:1276 – 1279.
- Smith R. What clinical information do doctors need? BMJ 1996; 313:1062- 1068.
- Ely JW, Levy BT, Hartz A. What clinical information resources are available in family physicians´ office. J Fam Pract 1999; 48: 135 – 139.
- Sibley JC, Sackett DL, Neufeld V, et al. A randomised trial of continuing medical education. N Engl J Med 1982; 306: 511 – 5.
- Ramsey PG, Carline JD, Inui TS, Larson EB, et al. Changes Over Time in the Knowledge Base of Practicing Internists. JAMA 1991; 266(8): 1103 – 7.
- General Medical Council. Tomorrow’s doctors. Recommendations on undergraduate medical education. London: GMC, 1993.
- Sackett DL, Haynes RB, Taylor DW, et al. Clinical determinants of the decision to treat primary hypertension. Clinical Research 1977; 24:648.
- Shaughnessy AF, Slawson DC. Are we providing doctors with the training and tools for lifelong learning? BMJ 1999; 319: 1280.
- Evidence Based-Medicine: a new paradigm for the patient. JAMA 1993; 269: 1253 –54.
- Neufeld VR, Barrows HS. The “McMaster philosophy”: an approach to medical education. J Med Edu 1974;49: 1040 – 1050.
- Gol JM. Bienvenidos a la medicina basada en la evidencia. En: La Medicina Basada en la Evidencia: Guías del usuario de la literatura médica. Evidence Based Medicine Working Group. JAMA.(Edición en Español) 1997.
- Shin JH, Haynes RB, Johnston ME. Effect of problem-based, self directed undergraduate education on life-long learning. Can Med Assoc J 1993;148:969 – 76.
- Ardila E y cols. Búsqueda manual de la literatura biomédica colombiana sobre intervenciones o terapias. Colaboración Cochrane en Español. Colombia 1999 – 2001.
- Isaacs D, Fitzgerald D. Seven alternatives to evidence based medicine. BMJ 1999; 319: 1618 – 1618.
- Sackett DL, Rosenberg WM, Gray JAM, Haynes RB, Richardson WS. Evidence Based Medicine: what it is and what is isn’t. BMJ 1996; 312:71-2.
- Haynes RB. The origin and aspirations of ACP Journal Club 1991; January / February: A 18.
- Oxman A, Guyatt GH. The science of reviewing research. Ann NY Acad Sci 1993; 703:125 – 34.
- Cochrane Collaboration. Cochrane Database of Systematic Review, 1st issue, 2000. BMJ Publishing Group, BMA House, Tavistock Square, London WC1H 9JR, UK.
- Browman GP, Levine MN, Mohide EA, Hayward RSA, Pritchard KI, Gafni A, Laupacis A. The Practice Guideline Development Cycle: A Conceptual Tool for Practice Guideline Development and Implementation. J Clin Oncol 1995; 13(2): 502 – 12.
- Davis DA, Thompson MA, Oxman AD, Haynes RB. Evidence for the effectiveness of CME: A Review of 50 Randomized Controlled Trials. JAMA 1992; 268 (9: 1111 – 17.
- Rennie D, Bero LA. Throw it away, SAM: The controlled Circulation Journals. CBE Views 1990; 13: 31 – 5.
- Bero LA, Galbraith A, Rennie D. The publication of sponsored symposiums in medical journals. N Engl J Med 1992; 327: 1135 – 40.
- Rennie D, Flanagin A. Publication bias: the triumph of hope over the experience . JAMA 1992; 267:411 – 412.
- Greenhalgh T. Getting your bearings. BMJ 1997; 315: 243 – 46.
- Jacobson LD, Edwards AG, Granier SK, Butler CC. Evidence-based medicine and general practice. Br J Gen Pract 1997; 47: 449 – 452.
- Greenhalgh T. The Medicine Database. BMJ 1997; 315:180-3
- Haynes RB, Wilczynski NL, McKibbon KA, Walker CJ, Sinclair JC. Developing optimal search strategies for detecting clinically sound studies in MEDLINE. J Am Med Assoc 1994;1:447 – 58.
- Slawson DC, Shaughnessy AF, Bennett JH. Becoming a medical information master: feeling good about not knowing everything. J Fam Pract 1994; 38: 505 – 13.
- Department of clinical Epidemiology and Bioestatistics, McMaster University Health Medical Centre. How to read clinical journals: I. Why to read them and how start reading them critically. Can Med Assoc J 1981; 124: 555 – 558.
- Oxman A, Sackett DL, Guyatt GH. User’s guides to the medical literature. I. How to get started. JAMA 1993; 270: 2093 – 5.
- Greenhalgh T. How to read a paper. The basics of evidence Based Medicine. London: BMJ Books, 1997.
- Riegelman RK, Hirsch RP. Cómo estudiar un estudio y probar una prueba: lectura crítica de la literatura médica. 2ª ed. Washington DC: OPS 1992 – 260p. (Publicación científica; 531).
- Guyatt GH, Sackett DL, Cook D, Evidence Based Medicine Group. How to use an article about therapy or prevention. A: Are the results of the study valid ?. JAMA 1993; 270:2598 – 2601.
- Guyatt GH, Sackett DL, Cook D, Evidence Based Medicine Group. How to use an article about therapy or prevention. What were the results and will they help me in caring for my patients?. JAMA 1994; 271:59-63.
- Jaeschke R, Guyatt GH, Sackett DL, Evidence Based Medicine Group. How to use an article about a diagnostic test: A: Are the results of the study valid?. JAMA 1994; 271:389 – 391.
- Jaeschke R, Guyatt GH, Sackett DL, Evidence Based Medicine Group. How to use an article about a diagnostic test: B. What were the results and will they help me in caring for my patients?. JAMA 1994; 271:703 – 7.
- Levine M, Walter S, Lee H, Haines, et al. Evidence Based Medicine Group. How to use an article about harm. JAMA 1994; 271: 1615 – 19.
- Laupacis A, Wells G, Richardson S, Tugwell P, Evidence Based Medicine Group. How to use an article about prognosis. JAMA 1994; 272:234 – 37.
- Oxman AD, Cook DJ, Guyatt G, Evidence Based Medicine Group. How to use an Overview. JAMA 1994;272: 1367 – 71.
- Richardson WS, Detsky AS, Evidence Based Medicine Group. How to use a Clinical Decision Analysis. A: Are the results of the study valid?. JAMA 1995; 273:1292 – 95.
- Richardson WS, Detsky AS, Evidence Based Medicine Group. How to use a Clinical Decision Analysis. B. What were the results and will they help me in caring for my patients?. JAMA 1995; 273:1610 – 13.
- Drummond MF, Richardson W, O´Brien B, Levine M, Heyland D, Evidence Based Medicine Group. How to use an Article on Economic Analysis of Clinical Practice. A: Are the results of the study valid?. JAMA 1997; 277:1552 – 57.
- Drummond MF, Richardson W, O’Brien B, Levine M, Heyland D, Evidence Based Medicine Group. How to use an Article on Economic Analysis of Clinical Practice. B. What were the results and will they help me in caring for my patients?. JAMA 1997; 277:1802 – 1806.
- Hayward RSA, Wilson MC, Tunis SR, Bass EB, Guyatt G, Evidence Based Medicine Group. How to use Clinical Practice Guideline. A: Are the recommendations valid?. JAMA 1995; 274:570 – 4.
- Hayward RSA, Wilson MC, Tunis SR, Bass EB, Guyatt G, Evidence Based Medicine Group. How to use Clinical Practice Guideline. B. What are the Recommendations and will they help you in caring for your patients?. JAMA 1995; 2747:1630 – 32.
- cheverry J, Pardo R. Estrategias de investigación clínica. Estudios observacionales: Reportes de Casos y Series de Casos. RCC Rev Col Cardiol 1999; 7(1):15 – 20.
- CooK DL, Guyatt GH, Laupacis A, et al. Rules of evidence and clinical recommendations on the use of antithrombotics agents. Chest 1992;102:305S-311S.
- Sackett DL. Rules of evidence and clinical recommendations on the use of antithrombotics agents. Chest 1989;95:2S-4S.
- US Department of Health Services, Public Health Service. Agency for Health Care Policy and Research (1992).
- Rothman KJ. Types of Epidemiologic Studies. En: Rothman KJ. Modern Epidemiology. Boston: Little, Brown and Company, 1986:51-76. http//:cebm.com
- Gómez R. La Medicina: Una profesión. Pediatría 1999;34(4):245-50.

CLIC AQUÍ Y DÉJANOS TU COMENTARIO