Gastroenterología. XVI no. 4
Lo más reciente
Revista de Gastroenterología: Comité, Volumen XVI No. 4
DIRECTOR – EDITOR Luis Alejandro Orozco Linares [enc_su_row][enc_su_column size=”1/2″] Editores Asociados Mario Humberto Rey Tovar, Adriana Rengifo Pardo, Jorge Alberto...
Editorial: Carta del Presidente
Quiénes somos y Qué buscamos LUIS ALEJANDRO OROZCO LINARES DIRECTOR- EDITOR REVISTA COLOMBIANA DE GASTROENTEROLOGÍA. La Revista Colombiana de Gastroenterología...
Crónica: Salud y Educación
ADRIANA RENGIFO P., MD. GASTROENTERÓLOGA, PROFESORA AUXILIAR, DEPARTAMENTO DE MEDICINA INTERNA. UNIVERSIDAD DEL VALLE, CALI. Todas las sociedades modernas coinciden en...
Anemia Perniciosa
Trabajos Originales Presentación de casos y revisión de temas JULIÁN DAVID MARTÍNEZ, MARIO HUMBERTO REY T., JUAN CARLOS MOLANO, MARTÍN ALONSO...
Colonoscopia total en Pacientes con Diarrea Crónica
Trabajos Originales Evaluación de una Cohorte con Colitis Linfocítica y Colagenosa RODRIGO CASTAÑO LLANO, MD., CIRUGÍA GASTROINTESTINAL Y ENDOSCOPIA. PROFESOR...
Cuadro Clinico y Tratamiento de la Colonoscopia
Resultados Entre enero de 1998 y junio de 2001 se realizaron 1.466 colonoscopias, cuya indicación por diarrea crónica estaba claramente...
Casos de Colonoscopia en Pacientes con Diarrea Crónica
Discusión El término de colitis colagenosa (CC) fue acuñado por Lindstrom en 1976, para describir los cambios histológicos subepiteliales de...
Efectos de un Programa Psicoterapéutico, combinado a una Terapia Farmacológica
Trabajos Originales Tratamiento del Distrés Psicológico y a la Sintomatología Física de sujetos con Dispepsia no Ulcerosa (DNU) STEFANO VINACCIA, UNIVERSIDAD...
Procedimiento del Programa Psicoterapéutico
Procedimiento Evaluación Todos los sujetos fueron evaluados al comienzo y al final del tratamiento, para lo cual se tomó como...
Cambios Endosonográficos presentes en la Enfermedad de Hirschprung
Invitado Internacional Enfermedad de Hirschprung presentación de dos casos ROBERTO FOGEL, JOSÉ POLEO, IDALYS BONILLA, JUANA FRONTERA DE FOGEL GASTROENTERÓLOGOS...
Falla Hepática Fulminante
Actualización CARLOS GÓMEZ CARRASCAL, MÉDICO ESPECIALISTA EN GASTROENTEROLOGÍA Y HEPATOLOGÍA. UNIVERSIDAD AUTÓNOMA DE MADRID. ESPAÑA. Hablamos de falla hepática fulminante como...
Pronóstico y Tratamiento de la Falla Hepática Fulminante
Pronóstico En la supervivencia influyen en grado variable la intensidad del coma, la edad, el sexo, la etiología y las...
Tratamiento endoscópico de la úlcera péptica sangrante
Práctica del Experto William Otero R., Md. Medicina Interna, Gastroenterología, Epidemiología; Gastroenterología, Clínica Fundadores; Profesor De Gastroenterología, Universidad Nacional De...
Desarrollo e Investigación Clínica de un Medicamento
Rincón Epidemiológico PARTE I Jairo Andrés Martínez, Md. Médico Cirujano, Universidad El Bosque, Postgrado En Farmacología, Universidad Nacional De Colombia,...
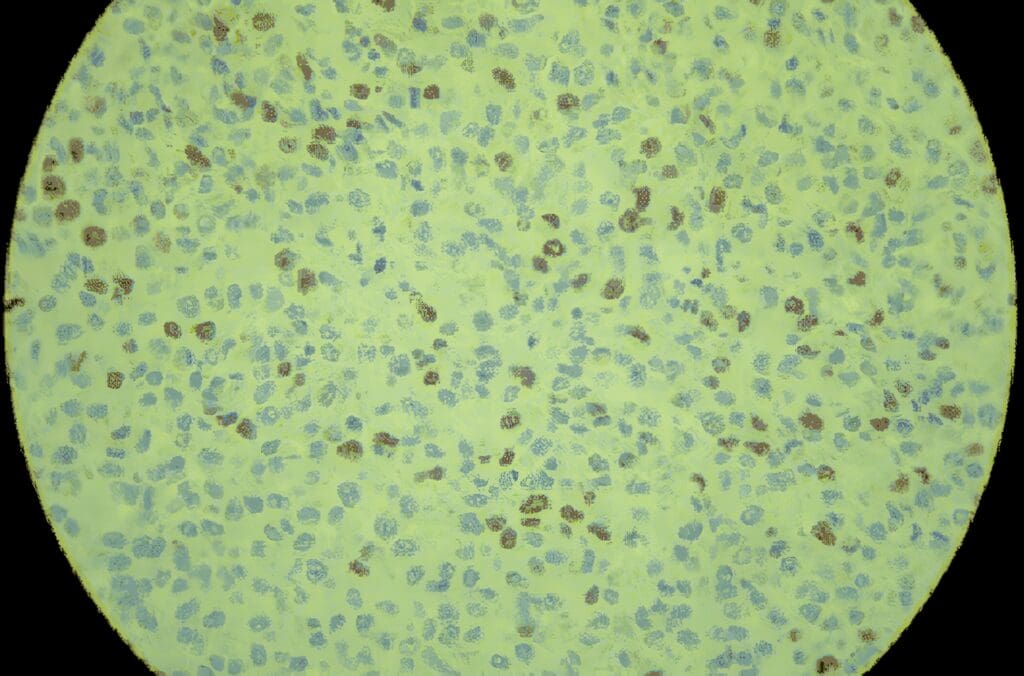
Caso Clínico Interinstitucional: Melanoma Anal
Reporte de dos Casos y Revisión del Tema José A. Hormaza L., Md. Especialista En Coloproctología, Profesor De Cirugía Colorrectal...
Discusión en Melanoma Anal
El melanoma anal (MA) es una entidad poco frecuente y de pobre pronóstico (1-3,9,10,20). Corresponde al 1-2% de las neoplasias...
Revista de Gastroenterología: Indicaciones a los Autores, Volumen XVI Nº 4
La Revista Colombiana de Gastroenterología (RCG ) como órgano oficial de las Asociaciones Colombianas de Gastroenterología, Endoscopia Digestiva, Coloproctología y...